
popular-science
打破吸收瓶颈的结晶封印术:姜黄素过饱和自纳米乳的诞生
姜黄素虽然被制成了自纳米乳以促进吸收,但在胃肠道中极易析出结晶而失效。科学家创新加入 Soluplus 聚合物,成功将药物维持在极其高效的“过饱和”状态。

姜黄素(Curcumin)因其卓越的抗炎抗癌功效备受瞩目,但它在水中的溶解度几乎为零,导致人体极难吸收。为了对付这个顽疾,药剂学家发明了“自纳米乳(SNEDDS)”——这是一种含有姜黄素的油相与乳化剂的混合液,当患者将其吞下肚子、遇到胃肠液时,它会自动在胃里变成纳米级的乳液,大幅提高溶解度。
但这个方案并不完美。在胃肠道里,当纳米乳液被稀释时,姜黄素经常会像盐巴一样重新结晶析出(沉淀)。一旦变成固体结晶,吸收率又会瞬间打回原形。如何阻止这些药物分子在胃里“抱团结晶”?

沉淀抑制剂:Soluplus 的降维打击
为了打破这个最后吸收瓶颈,科研团队决定在自纳米乳中加入一种名为“沉淀抑制剂(PPIs)”的秘密武器,将其升级为过饱和自纳米乳(SSNEDDS)。
在筛选了多种高分子聚合物后,一种名为 Soluplus 的新型材料脱颖而出。
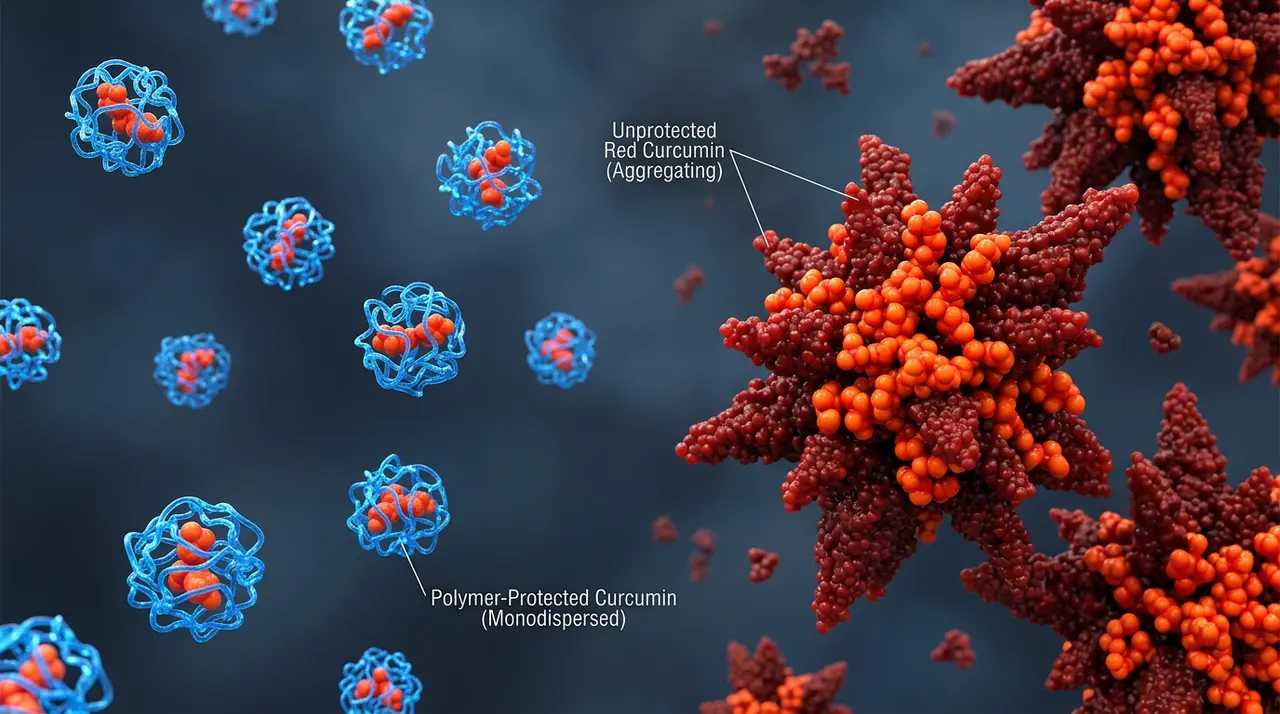
实验发现,Soluplus 就像是一个极具黏性的微观保护网。当姜黄素纳米乳在人工胃肠液中扩散、药物浓度远超其溶解度(达到“过饱和”状态)、眼看就要结晶析出时,Soluplus 的高分子长链会迅速缠绕住游离的姜黄素分子。它通过空间位阻和分子间的相互作用,死死拖住了姜黄素分子,让它们无法聚集形成晶核。
维持 2 小时的吸收黄金期
有了 Soluplus 的加持,数据的表现堪称惊艳。
在体外的溶出测试中,普通的自纳米乳在稀释后,姜黄素的过饱和状态很快崩溃,大量药物沉淀析出。而加入 Soluplus 的过饱和自纳米乳,竟然能在人工胃肠液中,将姜黄素的高浓度“过饱和状态”稳稳地维持长达 2 个小时以上(过饱和度维持在 10 以上)!
这 2 个小时,正是药物在肠道中被吸收的黄金时间窗口。
口服给药技术的巅峰之作
这项研究利用物理化学的高端手段,完美地解决了一个极其棘手的药剂学难题。
“过饱和自纳米乳”不仅保留了原技术遇水瞬间纳米化的高效性,更通过添加沉淀抑制剂,为极其难溶的中药有效成分(如姜黄素)打造了一个强力且持久的液体吸收环境。这标志着难溶性中药提取物的口服给药技术,向着更高的临床生物利用度迈出了关键的一大步。
下方为可供下载的参考 PDF,仅供学习交流;引用格式与页码请以正式出版物为准。